A krónikus gyulladás biológiai mechanizmusai és következményei
Blog
A krónikus gyulladás biológiai mechanizmusai és következményei
Szerző: Dr. Szabó Zsófia, oxyológus szakorvos, IBLM életmódorvos
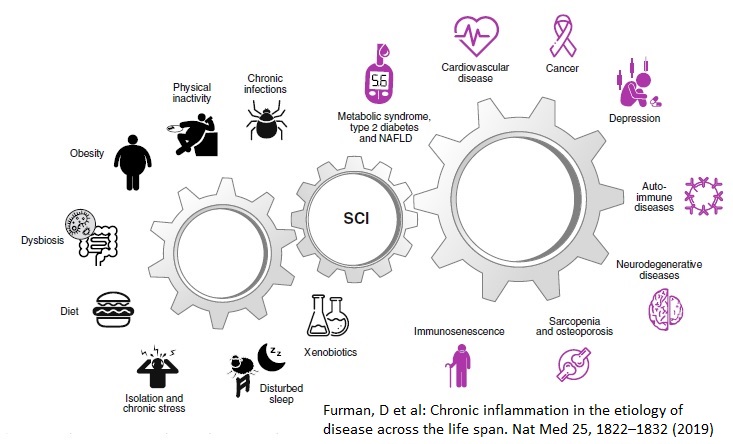
Az orvostudomány elmúlt két évtizedének egyik mérföldköve az a felismerés volt, hogy a szervezet immunrendszere – és ezen belül a gyulladásos folyamatok – nem csupán specifikus kórképekben játszanak szerepet, hanem a népbetegségek szinte teljes spektrumában. Bár sérülések és fertőzések során a gyulladásos aktivitás átmeneti emelkedése alapvető túlélési mechanizmus, a modern kutatások azt igazolták, hogy bizonyos hatások szisztémás krónikus gyulladást (systemic chronic inflammation SCI) indukálhatnak. Ez az állapot a krónikus megbetegedések elsődleges hajtóereje lehet: egyes becslések szerint globálisan a halálesetek akár 50%-a gyulladás mediált folyamatokra vezethető vissza, például a koszorúér-betegségek, a stroke, a malignus daganatok, a cukorbetegség, a metabolikus eredetű zsírmáj (metabolic dysfunction associated steatotic liver disease – MASLD), valamint számos neurodegeneratív és autoimmun kórkép. A krónikus gyulladás kialakulásának kockázata egészen az élet korai szakaszáig – akár a születésünk előtti korig – visszavezethető, és hatásai jelen ismereteink szerint az egész életen át fennmaradnak, befolyásolva a felnőttkori egészséget és a halálozási kockázatot.
A gyulladásos folyamat egy fertőzésre vagy sérülésre adott természetes válaszreakció, melynek során az immun- és nem-immunsejtek összehangolt aktivációja zajlik. Célja a homeosztázis helyreállítása, a szervezet egészségének megőrzése, a kórokozók eltávolítása és a szöveti regeneráció elősegítése. A gyulladásos válasz kiterjedésétől függően – legyen az lokális vagy szisztémás – jelentős anyagcsere- és hormonális változások következnek be. Ezek a folyamatok a szervezet energiáját és anyagcseréjét az immunrendszer működésének támogatására irányítják.
A fiziológiás gyulladásos választ alapvetően annak időbeli korlátozottsága jellemzi: a válaszreakció a fenyegetés megjelenésekor kezdődik, majd a veszély elhárításával párhuzamosan maradéktalanul lecseng.
Noha bizonyos molekuláris mechanizmusokban átfedést mutatnak, az akut gyulladásos válasz és a szisztémás krónikus gyulladás alapvetően eltérő folyamatok. Az akut választ jellemzően fertőző ágensek indukálják. A folyamat a veleszületett immunrendszer mintázatfelismerő receptorai (pattern recognition receptor – PRR) és a kórokozók bizonyos struktúrái, az úgynevezett kórokozó-asszociált molekuláris mintázatok (pathogen-associated molecular patterns – PAMP) közötti kapcsolattal veszi kezdetét. Ezen receptorok aktiválódása olyan fehérjék – citokinek, kemokinek és növekedési faktorok – tömeges növekedését eredményezi, melyek koordinálják a szervezet immunválaszát. Ezek a molekulák összehangolják a veleszületett és az adaptív immunrendszer munkáját, elősegítve a kórokozók (pl. baktériumok, vírusok) eltávolítását, valamint aktiválják a szöveti regenerációért és a teljes gyógyulásért felelős javító mechanizmusokat.
Ezzel szemben a krónikus gyulladást jellemzően kémiai vagy anyagcsere-eredetű káros ingerek, úgynevezett „steril” ágensek váltják ki. Ilyenek például a sérült sejtekből felszabaduló anyagok vagy környezeti toxinok, amelyeket összefoglaló néven veszély-asszociált molekuláris mintázatoknak (damage-associated molecular patterns -DAMP) nevezünk.A krónikus gyulladás mértéke erősen összefügg az életkorral: a klinikai vizsgálatok azt mutatják, hogy az idősebbeknél magasabb a keringő gyulladásos citokinek, az akut fázis fehérjék szintje, valamint a gyulladással kapcsolatos gének aktivitása. A krónikus gyulladás egy alacsony intenzitású, de permanens állapot, amely hosszú távon a szövetek és szervek irreverzibilis károsodásához vezethet.
A reaktív oxigéngyökök (reactive oxygen species – ROS) fontos szerepet játszanak a molekuláris folyamatokban. Egyrészt kiváltóként – például környezeti ártalmak vagy oxidált molekulák hatására – a DAMP fehérjéken keresztül indítják el a krónikus gyulladást, másrészt mint mediátorok részt vesznek a jelátviteli útvonalak működésében. A gyulladás folyamata során további ROS keletkezik melléktermékként, ami az úgynevezett „ördögi kör” részeként folyamatosan fenntartja a krónikus gyulladást.
Krónikus gyulladás és krónikus betegségeink kapcsolata
Ma már széles körben elfogadott, hogy az atherosclerosis kialakulásának szinte minden szakaszában kulcsszerepet játszik a krónikus gyulladás. Az endothelsejtek aktiválása elősegíti az immunsejtek érfalba jutását, a gyulladásos mediátorok pedig fenntartják a plakk növekedését, és elősegítik annak repedését, növelve a stroke vagy szívinfarktus kockázatát. A már kialakult szívizomelhalás újább gyulladásos kaszkádot indít el a sérült szövetek helyreállítása érdekében.
A zsírszövetből származó egyes gyulladásos citokinek hatással vannak számos inzulinjelátviteli útvonalra, így hozzájárulnak az inzulinrezisztencia kialakulásához és fenntartásához, mely a cukorbetegség és metabolikus szindróma fő kockázati tényezője. A már kialakult cukorbetegség egy krónikus, alacsony fokú gyulladásos állapotként írható le, amelyben a folyamatosan jelenlévő gyulladásos mediátorok (pl. TNF-α, IL-6, IL-1β) tovább rontják a szöveti inzulinrezisztenciát, valamint a glükóz anyagcsere zavarát. Ez a tartós gyulladás nemcsak az anyagcsere-zavarokat súlyosbítja, hanem elősegíti az érfali károsodást is, így közvetlen kapcsolatot teremt a diabétesz és a szív- és érrendszeri betegségek között. A cukorbetegségben szenvedők halálozásának és rokkantságának fő oka a szív- és érrendszeri megbetegedések, melyek a 2-es típusú cukorbetegeknél átlagosan 14,6 évvel korábban jelentkeznek. A cukorbetegségben szenvedők haláleseteinek körülbelül kétharmada szív- és érrendszeri betegségeknek tudható be; ezek közül körülbelül 40% ischaemiás szívbetegségben, és körülbelül 10% stroke-ban hal meg.
A krónikus gyulladás kritikus tényező a daganatos megbetegedések kialakulásában és progressziójában is. A daganatfejlődés minden szakaszát érinti, a kezdetektől és a progressziótól az invázióig és az áttétképződésig. Tartós gyulladás során a gyulladásos sejtek nagy mennyiségben termelnek reaktív oxigén- és nitrogénszármazékokat , amelyek közvetlenül károsíthatják a DNS-t, így növelik a genetikai instabilitást és mutációk felhalmozódását, ami rákos átalakuláshoz vezethet. A tumoros elváltozások emellett gyakran létrehoznak egy gyulladásos mikrokörnyezetet, amely lokálisan a növekédési faktorokkal és citokinekkel támogatják a rosszindulatú sejtek túlélését, és növekedését. A gyulladással szorosan összefüggő környezeti és életmódbeli tényezők jelentősen hozzájárulnak a rák előfordulásához. A krónikus fertőzések, a dohányzás, az elhízás és az étkezési szokások a globális rákteher nagy részét teszik ki. Ezek a tényezők fenntartják a tartós gyulladásos válaszokat, elősegítve azokat a körülményeket, amelyek genetikai mutációkat és a tumor progresszióját idézik elő. A folyamat komplexitás mutatja, hogy a gyulladás daganatellenes immunválaszt is aktiválhat, ezt a mechanizmust használják jelenleg a rák immunterápiájában.
Jól látható tehát, hogy a krónikus gyulladás egy komplex, önmagát fenntartó, minden szervrendszerre ható folyamat, amely jelentősen hozzájárul egészségünk alakulásához. Tartós fennállása felborítja az anyagcsere- és immunegyensúlyt, elősegítve a sejtkárosodást, szöveti funkciók romlását és számos krónikus betegség kialakulását. Mindez jól mutatja, hogy a krónikus gyulladás központi tényező a civilizációs betegségek kialakulásában, és indokolja a folyamat további kutatását, megismerését és megértését.
Li X, Li Y, Li L, et al. Inflammation in cardiovascular diseases: from pathogenesis to therapy. MedComm. 2025;6:e519. doi:10.1002/mco2.519.
Ridker PM, MacFadyen JG, Thuren T, et al. Residual inflammatory risk in atherosclerosis. Nat Med. 2020;26:1680–1691. doi:10.1038/s41591-019-0675-0.
Savi M, De Caterina R. The role of inflammation in cardiovascular disease: focus on cytokines and chemokines. Cureus. 2024;16:e319381. doi:10.7759/cureus.319381.
Shalapour S, Karin M. Immunity, inflammation, and cancer: an eternal fight. Oncotarget. 2017;8:23208–23225. doi:10.18632/oncotarget.23208.
Donath MY, Shoelson SE. Type 2 diabetes as an inflammatory disease. Nat Rev Immunol. 2011;11:98–107. doi:10.1038/nri2925.
Yao Y, Luo X, Li C, et al. Chronic inflammation and its impact on tissue homeostasis. Cells. 2025;14:488. doi:10.3390/cells14070488.


